国家药监局:16 家企业生产的 36 批次药品不符合规定
日前,国家药监局发布通告称,经江西省药品检验检测研究院等 4 家药品检验机构检验,标示为南京白敬宇制药有限责任公司等 16 家企业生产的 36 批次药品不符合规定。
其中,盐酸金霉素眼膏有 20 批次,重楼、地黄(熟地黄)、山药等共有 16 批次。对上述不符合规定药品,相关药品监督管理部门已要求相关企业暂停销售使用、召回产品,开展不符合规定原因调查,并切实深入进行整改。
不合规药品详情
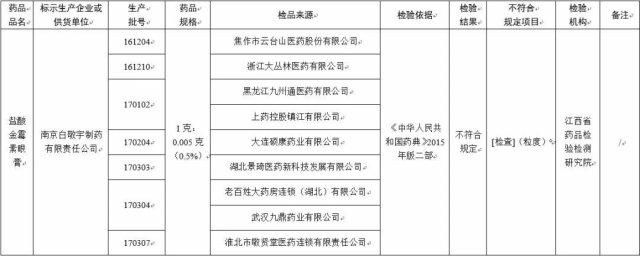
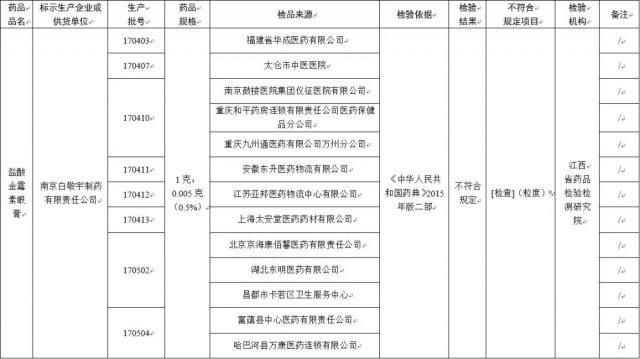
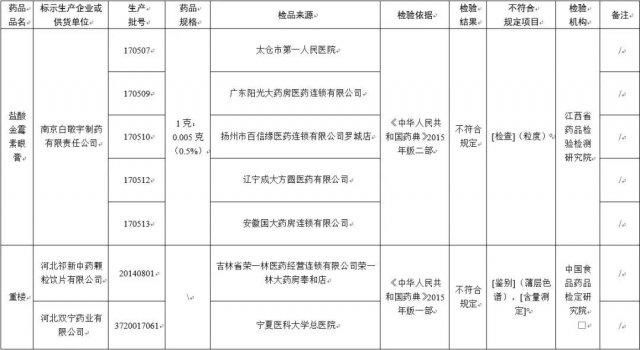
经江西省药品检验检测研究院检验,标示为南京白敬宇制药有限责任公司生产的 20 批次盐酸金霉素眼膏不符合规定,不符合规定项目为粒度。
经中国食品药品检定研究院检验,标示为河北祁新中药颗粒饮片有限公司、河北双宁药业有限公司生产的 2 批次重楼不符合规定,不符合规定项目包括薄层色谱、含量测定。
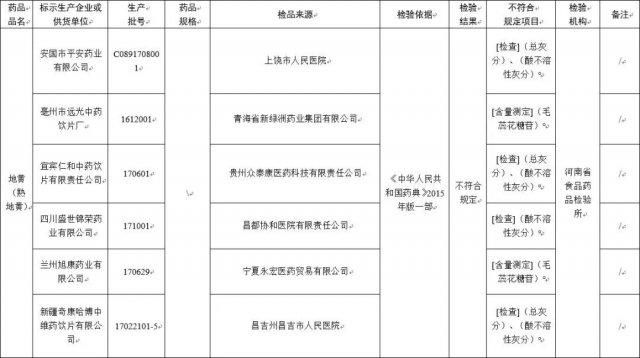
经河南省食品药品检验所检验,标示为安国市平安药业有限公司、亳州市远光中药饮片厂、宜宾仁和中药饮片有限责任公司、四川盛世锦荣药业有限公司、兰州旭康药业有限公司、新疆奇康哈博中维药饮片有限公司生产的 6 批次地黄不符合规定,不符合规定项目包括总灰分、酸不溶性灰分、含量测定。
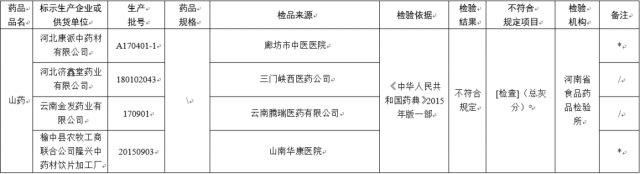
经河南省食品药品检验所检验,标示为河北济鑫堂药业有限公司、云南金发药业有限公司等 4 家企业生产的 4 批次山药不符合规定,不符合规定项目为总灰分。
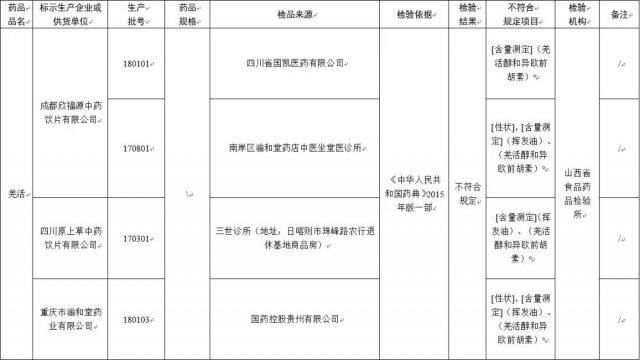
经山西省食品药品检验所检验,标示为重庆市渝和堂药业有限公司、成都欣福源中药饮片有限公司、四川原上草中药饮片有限公司生产的 4 批次羌活不符合规定,不符合规定项目包括性状、含量测定。(详见附件)
处置情况
对上述不符合规定药品,相关药品监督管理部门已要求相关企业暂停销售使用、召回产品,开展不符合规定原因调查,并切实深入进行整改。
国家药品监督管理局要求相关省级药品监督管理部门对上述企业和单位依据《中华人民共和国药品管理法》第七十三、七十四、七十五条等规定对生产销售假劣药品的违法行为进行立案调查,自收到检验报告书之日起 3 个月内完成对相关企业或单位的调查处理并公开处理结果。
36 批次不符合规定药品名单
备注:标" * "的药品为标示生产企业否认为该企业生产。
对上述不符合规定药品,相关药品监督管理部门已要求相关企业暂停销售使用、召回产品,开展不符合规定原因调查,并切实深入进行整改。
国家药品监督管理局要求相关省级药品监督管理部门对上述企业和单位依据《中华人民共和国药品管理法》第七十三、七十四、七十五条等规定对生产销售假劣药品的违法行为进行立案调查,自收到检验报告书之日起 3 个月内完成对相关企业或单位的调查处理并公开处理结果。
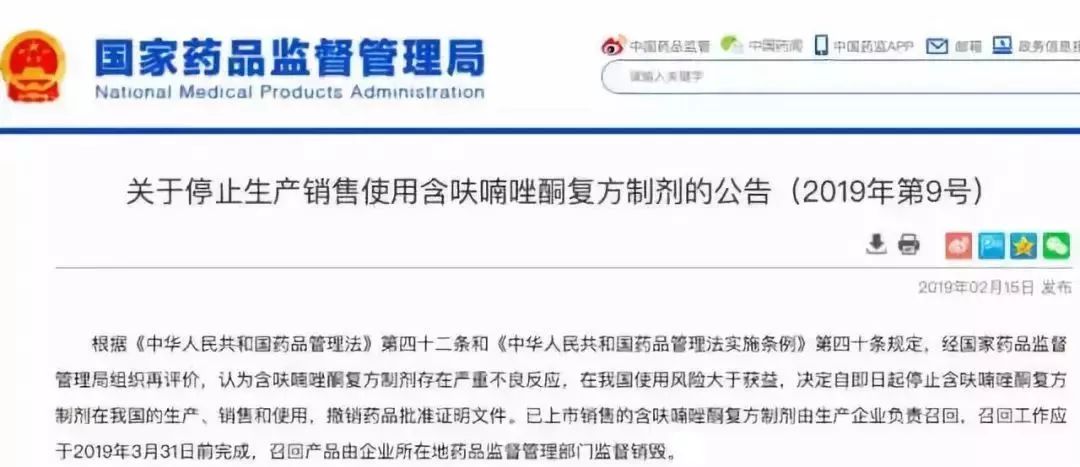
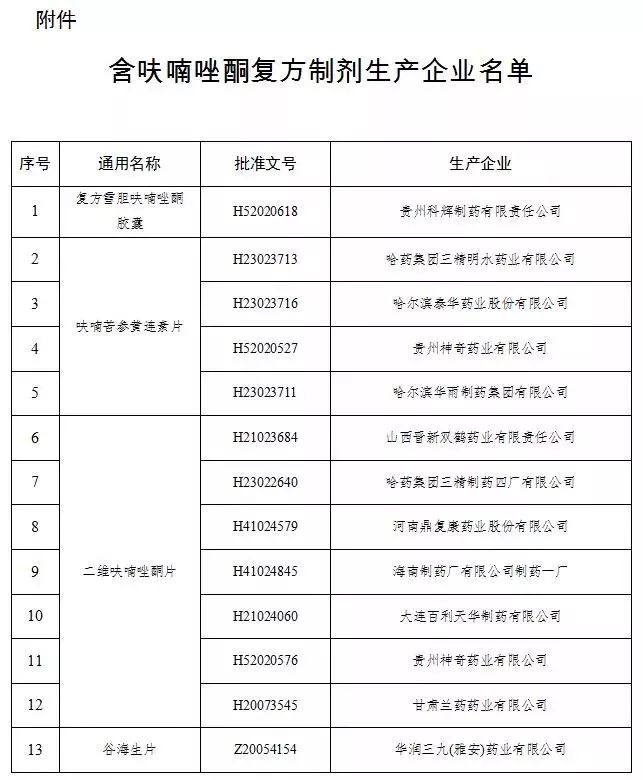
国家药品监督管理局2月15日发布公告称,自即日起停止含呋喃唑酮复方制剂的生产、销售和使用。目前,全国有12个制药公司、药厂生产此类相关药品。
根据《中华人民共和国药品管理法》第四十二条和《中华人民共和国药品管理法实施条例》第四十条规定,经国家药品监督管理局组织再评价,认为含呋喃唑酮复方制剂存在严重不良反应,在我国使用风险大于获益,决定自即日起停止含呋喃唑酮复方制剂在我国的生产、销售和使用,撤销药品批准证明文件。
已上市销售的含呋喃唑酮复方制剂由生产企业负责召回,召回工作应于2019年3月31日前完成,召回产品由企业所在地药品监督管理部门监督销毁。
这些药被紧急叫停
国家药监局给出了
四种禁用的含呋喃唑酮的复方制剂,
分别为
复方雪胆呋喃唑酮胶囊、
呋喃苦参黄连素片、
二维呋喃唑酮片、
谷海生片。
1、复方雪胆呋喃唑酮胶囊用于各种便秘以及由于腹腔炎症、肠粘连、肝胆疾病等的胃肠功能紊乱而引起的腹痛、食欲不振等;
2、呋喃苦参黄连素片为抗菌消炎药,用于急性菌痢,肠炎等;
3、二维呋喃唑酮片用于胃、十二指肠溃疡、慢性胃炎;
4、谷海生片用于消化性溃疡等。
这些药也都被叫停、禁用
2018年11月30日,
国家药监局发布
《关于停止生产销售使用特酚伪麻片
和特洛伪麻胶囊的公告(2018年第92号)》
特酚伪麻片和
特洛伪麻胶囊
国家药监局表示,根据《中华人民共和国药品管理法》第四十二条和《中华人民共和国药品管理法实施条例》第四十条规定,经组织再评价,认为:特酚伪麻片和特洛伪麻胶囊存在心脏毒性不良反应。
之前,国家药监局还公布了一系列,被限制使用的感冒药:
含可待因感冒药
18岁以下禁用
这类药包括:氨酚双氢可待因片、复方磷酸可待因糖浆、复方磷酸可待因口服溶液、磷酸可待因糖浆等,共计29 个批号。
双黄连注射剂
4周岁及以下儿童禁用
柴胡注射液
儿童禁用
修订要求在禁忌项下须列出“儿童禁用”,并增加警示语“本品不良反应包括过敏性休克”等。
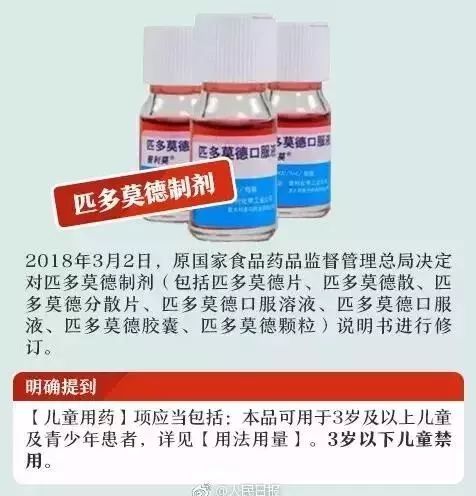
匹多莫德制剂
3岁以下儿童禁用
另外,
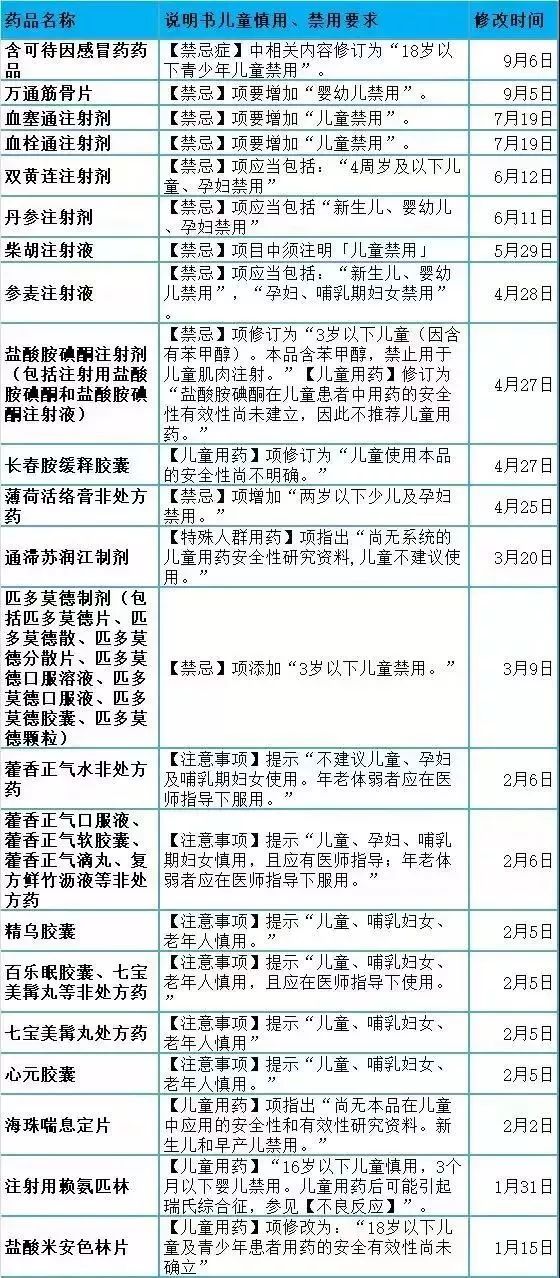
关于一些药品对儿童限用、
慎用的汇总如下:
大家家中有这种药或是,以前有服用过这种药的吗?
快转给身边人,检查一下家里有没有!